المجموعات الكيميائية
تمهيد:
درست سابقا أنه حينما تفقد ذرة العنصر الواحدة إلكتروناً أو إلكترونات تتحول إلى أيون موجب مثل (أيون الكالسيومCa+2) ، وحينما تكسب الذرةإلكتروناً أو إلكترونات تتحول إلى أيون سالب مثل(Br-1) .
تعرف هذه الأيونات العنصرية باسم الأيونات البسيطة تمييزاً لها عن أيونات تتكون من عدة ذرات ومن نوعين أو أكثر من العناصر ، ومن الأمثلة المعروفة لك في هذا المجال أيون الهيدروكسيدOH-1) ) ، وأيون الكبريتات(SO4-2) ، وأيون الأمونيوم (NH4+1) وغيرها، وتسمى هذه الأيونات باسم الأيونات المعقدة أو المجموعات الكيماوية .
درست سابقا أنه حينما تفقد ذرة العنصر الواحدة إلكتروناً أو إلكترونات تتحول إلى أيون موجب مثل (أيون الكالسيومCa+2) ، وحينما تكسب الذرةإلكتروناً أو إلكترونات تتحول إلى أيون سالب مثل(Br-1) .
تعرف هذه الأيونات العنصرية باسم الأيونات البسيطة تمييزاً لها عن أيونات تتكون من عدة ذرات ومن نوعين أو أكثر من العناصر ، ومن الأمثلة المعروفة لك في هذا المجال أيون الهيدروكسيدOH-1) ) ، وأيون الكبريتات(SO4-2) ، وأيون الأمونيوم (NH4+1) وغيرها، وتسمى هذه الأيونات باسم الأيونات المعقدة أو المجموعات الكيماوية .
المجموعات الكيماوية :
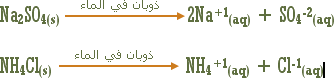
حينما نذيب مركبات معروفة مثل كبريتات الصوديوم الصلبة Na2SO4 ، وكلوريد الأمونيوم الصلب في الماء ، نحصل على أيونين فقط ، على الرغم من أن كل مركب منها يتكون من ثلاث عناصر، وإليك معادلة ذوبان هاتين المادتين في الماء:
حينما نذيب مركبات معروفة مثل كبريتات الصوديوم الصلبة Na2SO4 ، وكلوريد الأمونيوم الصلب في الماء ، نحصل على أيونين فقط ، على الرغم من أن كل مركب منها يتكون من ثلاث عناصر، وإليك معادلة ذوبان هاتين المادتين في الماء:
 |
تدريب (1) :
|
أيون الصوديوم Na+1
|
أيون النحاس Cu+2
|
أيون الكربونات CO3-2
|
أيون الأمونيوم NH4+1
|
أيون الألمنيوم Al+3
|
أيون النيترات NO3-1
|
أيون الكلوريد Cl-1
|
أيون البيرمنغنات MnO4-1
|
أيون الحديد Fe+3
|
أيون الخلات CH3COO-1
|
أيون الأوكسيد O-2
|
أيون الفوسفات PO4-3
|
ليست هناك تعليقات:
إرسال تعليق